【药品名称】
通用名称:甲硫酸新斯的明注射液
英文名称:Neostigmine Methylsulfate Injection
汉语拼音:Jialiusuan Xinsidiming Zhusheye
【成 分】本品活性成份为甲硫酸新斯的明。
化学名称:N,N,N-三甲基-3-[(N,N-二甲氨基)甲酰氧基]苯铵硫酸单甲酯盐。
化学结构:
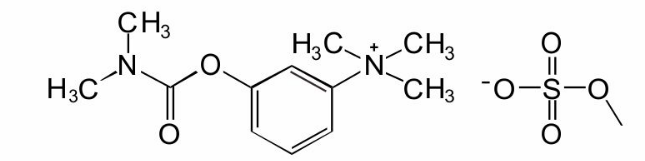
分子式:C13H22N206S
分子量:334.39
辅料:氯化钠(供注射用)、枸橼酸钠、枸橼酸、注射用水。
【性 状】本品为无色的澄明液体。
【适应症】抗胆碱酯酶药。用于手术结束时拮抗非去极化肌肉松弛药的残留肌松作用,用于重症肌无力,手术后功能性肠胀气及尿潴留等
【规 格】(1)1ml:0.5mg; (2)2ml:1mg
【用法用量】
常用量,皮下或肌内注射,一次0.25~1mg,一日1~3次。
极量,皮下或肌内注射,一次1mg,一日5mg。或遵医嘱。
【不良反应】
本品可致药疹,大剂量时可引起恶心、呕吐、腹泻、流泪、流涎等,严重时可出现共济失调、惊厥、昏迷、语言不清、焦虑不安、恐惧甚至心脏停搏。其他详见说明书。
【禁 忌】
1.对本品中任何成份过敏者禁用。
2.癫痫、心绞痛、室性心动过速、机械性肠梗阻或泌尿道梗阻及哮喘病人禁用。
3.心律失常、窦性心动过缓、血压下降、迷走神经张力升高禁用。
4.正在使用或应用去极化型肌松药(琥珀胆碱)的患者禁用
【注意事项】
1.慎用(下列患者需慎用本药)
(1)支气管喘息患者“有收缩支气管平滑肌作用”
(2)甲状腺功能亢进患者“有加剧甲状腺功能亢进症的风险
(3)冠状动脉梗塞患者“有收缩冠状动脉的可能"
(4)心动过缓患者“有增加过缓程度的风险"
(5)消化性渍疡患者“有可能增强胃酸分泌
(6)癫痫患者“有增加骨骼肌紧张,增强痉挛症状的风险”
(7)帕金森综合征患者“有增加不随意运动的风险"
(8)重度肾功能降低患者“有可能导致本药剂排泄迟缓,作用持续和增强的风险”
2.偶然会发生肌无力症状的严重恶化、呼吸困难、吞咽困难(危象)情况,此类情况下,应通过临床症状鉴别危象,如鉴别困难的,可静脉注射2mg依酚氨铵氯化物,鉴别危险后采取下列措施:
(1)胆碱能危象:出现腹痛、腹泻、出汗、唾液分泌过多、瞳孔缩小、抽搐等症状或使用依酚氧铵氧化物后症状加重或无变化时,应立即停止用药,静脉注射0.5~1.0mg硫酸阿托品水合物,并根据需要采取措施确保气管通畅。
(2)重症肌无力危象:当出现呼吸困难、排唾液困难、发绀、全身无力等症状时,或者服用依酚氯铵氯化物后症状得到改善时,可适当增加本药剂服用量。
3.本品用于对抗非去极化型肌松药(简箭毒碱、泮库溴铵、维库澳铵等)时,应注意:
(1)本品应先通过肌肉松弛监控确认其恢复或出现自发性呼吸后方可使用。
(2)如有心动过缓的情况,在服用本药剂之前,应先使用阿托品适当增加心率后再使用。
4.其他注意事项
(1)钙拮抗剂(地尔硫卓)用药中的患者使用甲硫酸新斯的明,偶有房室传导阻滞现象的报告。
(2)β阻断剂(阿替洛尔、普萘洛尔)用药中的患者使用甲硫酸新斯的明,偶有心动过缓、低血压现象的报告。
(3)具有神经肌肉阻断作用的氨基糖苷类、肽类等药物因为有肌肉松弛作用,有可能减弱本品的肌松药对抗作用。
(4)肺泡内氟烷浓度偏高的情况下不得使用本药剂。
【药物相互作用
1.本品有增强去极化肌肉松弛剂的作用,禁止与去极化型肌松药合用。
2.某些能干扰肌肉传递的药物如奎尼丁,能使本品作用减弱,不宜合用。
3.与胆碱能药物乙酰胆碱、萘二磺酸乙乳胆碱等合用时可增强相互作用,联合应用时应谨慎。
4.副交感神经抑制药物会掩盖胆碱能危象的初期症状,有导致过度用药的危险,因此与硫酸阿托品水合物、东莨菪碱氢溴酸盐、布托溴铵等联用时应谨慎。
【药理毒理】
药理作用
甲硫酸新斯的明是一种竞争性胆碱酯酶抑制剂。甲硫酸新斯的明通过减少乙酰胆碱的分解,诱导突触间隙中与非去极化神经肌肉阻滞剂竞争结合相同位点的乙酰胆碱的增加,逆转神经肌肉阻滞。
毒理研究
遗传毒性
甲硫酸新斯的明在Ames试验、体外中国仓鼠卵巢细胞染色体畸变试验、小鼠体内骨髓微核试验中结果为阴性。
生殖毒性
在大鼠生育力和早期胚胎发育毒性试验中,雄性大鼠于交配前静脉给药28天、雌性大鼠于交配前静脉给药14天,甲硫酸新斯的明的给药剂量折算为人体等效剂量(按体表面积计算)分别为1.6、4、8.1μg/kg/天,未见不良影响。
在胚胎-胎仔发育毒性试验中,大鼠和兔于器官发生期(大鼠妊娠第6天至第17天,兔妊娠第6天至18天)给予甲硫酸新斯的明,给药剂量折算为人体等效剂量(按体表面积计算)分别为1.6、4、8.1μg/kg/天和3.2、8.1、13μg/kg/天,在轻微母体毒性(震颤、共济失调和俯卧)的情况下,对大鼠和兔未见致畸性。
在大鼠围产期毒性试验中,大鼠于妊娠第6天至哺乳期第20天给予甲硫酸新斯的明,第21天离乳,给药剂量折算成人体等效剂量为1.6、4、8.1μg/kg。在轻微母体毒性(震颤、共济失调和虚脱)的情况下,对子代的身体发育、行为、学习能力或生育力未见不良影响。以上这些试验中动物的暴露量远低于人体预期暴露量。致癌性
尚未进行长期动物试验以评估新斯的明的致癌性。
【贮 藏】遮光,密闭,不超过30℃保存。
【包 装】中硼硅玻璃安瓿;10支/盒。
【有效期】24个月
【执行标准
【批准文号】(1)1ml:0.5mg 国药准字H20244008
(2)2ml:lmg 国药准字H20244009
【生产企业】
企业名称:山西诺成制药有限公司
生产地址:山西省怀仁市高新技术工业园区








